Сыпь при гемофильной инфекции
Гемофильная инфекция — острые инфекционные болезни, вызванные гемофильной палочкой. Гемофильная инфекция характеризуется преимущественным поражением органов дыхания, центральной нервной системы и развитием гнойных очагов в различных органах.
Этиология[править | править код]
Возбудитель — Haemophilus influenzae (палочка Пфайфера) относится к семейству Pasteurellaceae, роду гемофилюсов (который включает 16 видов бактерий).
Впервые гемофильная палочка инфлюэнцы была выделена Рихардом Пфайффером во время пандемии гриппа в 1889 году и была ошибочно принята за этиологическую причину гриппа, что и определило её название (бацилла Пфайффера). В 1920 г Винслоу и коллегами, открывшими необходимость для роста микроорганизма эритроцитарных факторов, была переименована в Haemophilus («любящая кровь»). В 1933 году была открыта вирусная природа гриппа, однако название influenzae сохранилось. Микробиологические и иммунологические свойства H. influenzae были открыты М.Питтман в 1930 году. В 1933 году Фотергиллом и Райтом была обнаружена зависимость заболеваемости гемофильной инфекцией от возраста.
Представляет собой мелкую грамотрицательную коккобациллу (0,3 мкм в диаметре), для своего роста требует наличия содержащихся в эритроцитах термолабильного фактора V (НАД) и термостабильного фактора X (гемин).
По культуральным свойствам (продукция индола, активность уреазы и др.) разделяется на 7 биотипов (от I до VII). Часть выделенных со слизистых оболочек палочек инфлюэнцы имеет капсулы. Известно 6 антигенно различающихся капсульных типов, обозначаемых от А до F. Наибольшее значение в патологии человека имеет Haemophilus influenzae type b. Данный серотип отличается от других наличием 8 генов, ответственных за образование фимбрий, которые способствуют улучшению адгезивных и пенетрантных свойств. Также, в отличие от других серотипов, гемофилюс инфлюэнцы типа b — единственно способная проникать в кровеносное русло.
Эпидемиология[править | править код]
Источником и резервуаром инфекции является только человек. Путь распространения — воздушно-капельный. Возбудитель локализуется на слизистой оболочке верхних дыхательных путей. H.influenzae можно выделить из носо-глотки 90 % здоровых людей, причем на более вирулентный тип b приходится около 5 % всех выделенных штаммов. Здоровое носительство может продолжаться от нескольких дней до нескольких месяцев. Носительство сохраняется даже при высоком титре специфических антител и даже при назначении высоких доз антибиотиков. Чаще всего заболевают дети в возрасте от 6 мес до 4 лет, реже болеют новорожденные, дети более старшего возраста и взрослые.
До введения обязательной вакцинации против Hib в США (до 1990г), по данным ААР (American Academy of Pediatrics) ежегодно отмечалось около 20000 случаев заболевания и около 1000 летальных исходов у детей в результате гемофильной инфекции. Неврологические осложнения отмечались в 25-35 % случаев.
В настоящее время в европейских странах регистрируется 26-43 случаев заболеваний на 100000 детей, смертность составляет 1-3 %, высок уровень неврологических осложнений.
Показатели заболеваемости гемофильной инфекцией типа b в тысячи раз выше у детей восприимчивых возрастов (75-85 % случаев заболеваний — в возрасте до 24 мес, пик — 6-12 мес).
Выделяют следующие группы риска для данного заболевания:
- люди экстремальных возрастов (дети до 2-х лет, пожилые люди);
- дети, посещающие детские дошкольные учреждения. В одном из исследований было показано, что до 50 % инвазивных форм можно отнести за счёт посещения детских учреждений;
- дети на искусственном вскармливании. У детей до года, находящихся на искусственном вскармливании и не получающих небольших дополнительных количеств материнских антител с грудным молоком, особенно высок риск самых тяжелых форм ХИБ-инфекции — воспаления легких и менингита. Фактор грудного вскармливания является отчасти гипотетическим, так как до конца не ясен механизм воздействия на защиту от гемофильной инфекции. Здесь могут играть роль как питательные, так и иммунные факторы, находящиеся в грудном молоке. После иммунизации женщин полисахаридной вакциной на 36-39 неделях беременности было отмечено 20-кратное возрастание выделения специфических антител с грудным молоком в послеродовом периоде;
- представители неевропейских рас. Этот фактор риска также является достаточно спорным, однако многие исследования заболеваемости показывали, что заболеваемость среди детей неевропейских рас значительно выше;
- лица с низким социально-экономическим статусом. Риск заболевания значительно увеличивается при скученном проживании;
- лица с различными видами иммунодефицита;
- крайне ослабленные и страдающие алкоголизмом;
- больные лимфогранулематозом (болезнь Ходжкина), серповидно-клеточной анемией;
- лица подвергшиеся спленэктомии (удаления селезёнки).
Заболеваемость повышается в конце зимы и весной. За последние годы заметно увеличилась заболеваемость взрослых.
Необходимо отметить, что вариант клинической формы гемофильной инфекции зависит от возраста. Так, согласно зарубежным данным, менингит встречается чаще у детей в возрасте 6-9 месяцев, эпиглоттит встречается чаще у детей старше 2-х лет, целлюлит (воспаление подкожной клетчатки) чаще встречается у детей в годовалом возрасте. Для взрослых и пожилых людей менингит является нехарактерным — чаще встречается пневмония.
Патогенез[править | править код]
Воротами инфекции является слизистая оболочка носоглотки. Механизмом передачи является воздушно-капельный, однако у маленьких детей путь передачи может быть контактным. Возбудитель может длительное время персистировать в области ворот инфекции в виде латентной бессимптомной инфекции. В некоторых случаях, в основном у лиц с ослабленными защитными силами и лиц, входящих в группу риска, латентная форма переходит в манифестную. Риск перехода инаппарантного носительства в манифестную форму усиливается при наличии сопутствующей вирусной инфекции и повышении микробной массы.
Необходимо отметить роль вторичных контактов. Данный механизм передачи наиболее актуален для детей в возрасте до двух лет. Следует отличать первичное заболевание, которое возникает вследствие контакта со здоровым носителем и вторичное, которое возникает при контакте с больным в манифестной форме.
Инфекция распространяется по окружающим тканям, обусловливая развитие синуситов, отитов, бронхитов, пневмоний, воспаление подкожной жировой клетчатки, или путём гематогенной диссеминации поражает суставы и другие органы, протекая по типу сепсиса. Штаммы гемофильной палочки, не имеющие капсулы, поражают только слизистые оболочки.
Системные заболевания вызывают только возбудители, обладающие капсулой, в 95 % случаях это гемофильная палочка типа b. Уникальным свойством бактерий данного типа является их способность проникать в кровеносное русло путём разрывания межклеточных соединений. Также, более выраженная патогенность этих штаммов связана с тем, что капсула способна подавлять фагоцитоз. Возбудитель может в течение нескольких суток персистировать в кровеносном русле бессимптомно до тех пор, пока масса микробных тел не станет критической. Затем бактерия проникает в ЦНС через хороидальные сплетения, вызывая инфильтрацию и гнойное воспаление мягких мозговых оболочек.
У перенесших заболевание развивается стойкий иммунитет.
Иммунный отклик организма на данный вид инфекции имеет несколько особенностей. Вследствие подавления фагоцитоза, продукция антител В-лимфоцитами активируется без участия Т-хелперов. Именно поэтому иммунный отклик организма в ответ на инвазию Hib в большинстве случаев недостаточен, отсутствует т. н. бустерный (ударный) отклик при повторной экспозиции антигена гемофильной палочки. Также отмечается крайне слабая Т-независимая продукция специфических антител в возрасте до 18 месяцев. Кроме того, полисахариды являются набором олигосахаридов, каждый из которых способен индуцировать слабый иммунный отклик. Это в свою очередь обусловливает множественность и вариабельность продуцируемых антител в ущерб количественному фактору.
Местный иммунитет, представленный секреторными антителами класса IgA изучен недостаточно. Более того, было обнаружено, что капсульные виды H.influenzae выделяют протеазы, инактивирующие антитела. Проведенные исследования местного иммунитета у здоровых носителей показали, что роль местного иммунитета может быть достаточно важной — блокировка пенетрации слизистой оболочки бактериями, предотвращение проникновения микроорганизмов в кровеносное русло.
Комплемент при гемофильной инфекции может быть активирован как по классическому (антитело-зависимому) пути, так и по альтернативному пути. Антигены клеточной стенки H.influenzae способны активировать комплемент по альтернативному пути, в то время как комплекс антител и антигенов, способен активировать комплемент по классическому пути.
Симптомы и течение[править | править код]
Длительность инкубационного периода установить трудно, так как заболевание нередко является следствием перехода латентной инфекции в манифестную. Может развиться местный воспалительный процесс слизистой оболочки верхних дыхательных путей или развиваются заболевания, обусловленные гематогенной диссеминацией. Гемофильная палочка типа b является одной из частых причин генерализованной инфекции (бактериемии) у детей, у половины из них развивается гнойный менингит, довольно часто (15-20 %) пневмония и реже другие очаговые поражения. Как правило, гемофильная инфекция протекает остро, но некоторые клинические формы могут принимать затяжное течение.
Гемофильная инфекция может протекать в следующих клинических формах:
- Гнойный менингит.
- Острая пневмония.
- Септицемия.
- Воспаление подкожной клетчатки (целлюлит).
- Эпиглоттит (воспаление надгортанника).
- Гнойный артрит.
- Прочие заболевания (перикардит, синуситы, отит, заболевания дыхательных путей и др.).
По данным Бостонского университета самыми частыми клиническими формами гемофильной инфекции являются менингит, средний отит и пневмония.
Гнойный менингит наблюдается преимущественно у детей от 9 месяцев до 4 лет (для данной возрастной группы это самая частая причина менингитов). Заболевание развивается остро, иногда с симптомов ОРЗ, затем быстро развивается клиническая симптоматика, характерная для бактериальных менингитов. Иногда менингиальный синдром сочетается с другими проявлениями гемофильной инфекции (гнойный артрит, воспаление надгортанника, целлюлиты. Заболевание протекает тяжело и нередко кончается летально (около 10-15 % случаев).
Гемофильная пневмония (по данным Бостонского университета) является второй по частоте среди всех бактериальных пневмоний у детей. Может проявляться как в виде очаговой, так и в виде долевой (крупозной), очень часто (до 70 %) сопровождается гнойным плевритом (у детей), может осложняться гнойным перикардитом, средним отитом. Может принимать затяжное течение. У взрослых, особенно пожилых лиц, гемофильная инфекция может наслаиваться на другие виды инфекции.
Гемофильный сепсис чаще развивается у детей 6-12 мес, предрасположенных к этому заболеванию. Протекает бурно, нередко как молниеносный, с септическим шоком и быстрой гибелью больного.
Воспаление подкожной клетчатки (целлюлит) также развивается у детей до 12 мес, чаще локализуется на лице, реже на конечностях. Начинается нередко с картины ОРЗ (ринофарингит), затем появляется припухлость в области щеки или вокруг глазницы, кожа над припухлостью гиперемирована, с цианотичным оттенком, иногда заболевание сопровождается воспалением средним отитом. Температура тела субфебрильная, симптомы общей интоксикации выражены слабо. У детей старших возрастов воспаление подкожной клетчатки может локализоваться на конечностях.
Воспаление надгортанника (эпиглоттит) является очень тяжелой формой гемофильной инфекции, в большинстве случаев (около 90 %) сопровождается бактериемией. Начинается остро, характеризуется быстрым подъёмом температуры тела, выраженной общей интоксикацией и картиной быстро прогрессирующего крупа, который может привести к гибели ребёнка от асфиксии (полная непроходимость дыхательных путей или остановка дыхания).
Гнойные артриты являются следствием гематогенного заноса гемофильной палочки, нередко сопровождаются остеомиелитом.
Диагноз, диффренциальный диагноз[править | править код]
При распознавании необходимо учитывать возраст больного, наличие факторов, способствющих инфицированию гемофильной палочкой, характерные клинические проявления (целлюлиты, эпиглоттит и др.). Подтверждением диагноза служит выделение гемофильной палочки в гное, мокроте, ликворе, материале, взятом со слизистых оболочек. Средами выбора для культивирования являются агары, обогащенные кровью (20 %)(желательно наличие эритроцитарных кофакторов X и V). Окраска по Граму также является диагностически важной.
Серологическими тестами выбора являются латекс-агглютинация и реакция преципитации. Ценность этих методов особенно велика для диагностики в тех случаях, когда антимикробная терапия была начата до посева культуры. В спинномозговой жидкости (иногда в моче) можно обнаружить капсульный антиген гемофильной палочки с помощью реакции встречного иммунофореза или иммуноферментного метода. Однако факт обнаружение не может однозначно свидетельствовать в пользу диагноза гемофильной инфекции, так как антиген может выявляться при носительстве, при недавней вакцинации полисахаридной вакциной или загрязнении анализа перекрестно-реагирующими фекальными микроорганизмами.
В клинически важных случаях проводят тест на антибиотикорезистентность.
Лечение[править | править код]
Без этиотропной терапии некоторые формы гемофильной инфекции (менингит, эпиглоттит) почти всегда заканчиваются смертью больного. Необходимо возможно раньше начать этиотропную терапию.
Наиболее эффективным и малотоксичным до 1970 года, когда был обнаружен факт наличия антибиотикорезистенности у H.influenzae, считался ампициллин, однако в последние годы всё чаще стали выделяться штаммы гемофильной палочки, резистентные к данному антибиотику. Ампициллин вводился внутривенно в суточной дозе 200—400 мг/кг/сут детям и 6 г/сут взрослым. Такие большие дозировки в назначении ампициллина обусловлены высокой резистентностью возбудителя к препарату. Исходя из этого ампициллин практически не используется в современной практике врачей. В некоторых рекомендациях, в частности в руководстве Американской Педиатрической Академии, предлагается с самого начала применять ампициллин, цефалоспорины в комбинации с левомицетином. Однако, согласно последним исследованиям, проведенным в России (Москве, Санкт-Петербурге и других крупных городах), штаммы гемофильной палочки, циркулирующие в этих регионах резистентны практически ко всем классам антимикробных препаратов.
В последнее время в отечественных и зарубежных публикациях появились сведения о более высокой, нежели для ампициллина, эффективности таких антибиотиков, как амоксициллин, цефалоспоринов — цефиксим и макролидов — азитромицин, даже при применении их короткими курсами. В Российской федерации только 2,8 % штаммов H.influenzae вырабатывают β-лактамазы, вследствие чего необходимость в использовании препаратов с клавулановой кислотой преувеличена (данные исследования ПеГАС 2014). Необходима консультация врача.
Профилактика и мероприятия в очаге[править | править код]
Здоровым носителям гемофильной палочки типа b и лицам из группы риска, контактирующим с больными гемофильной инфекцией, в течение первой недели после регистрации первого случая заболевания рекомендуется принимать рифампицин внутрь в дозе 10-20 мг/кг/сут (максимум 600 мг/сут) однократно в течение 4 дней.
Специфическая иммунопрофилактика[править | править код]
В 1974 году в Финляндии было проведено первое широкомасштабное исследование эффективности капсулярной полисахаридной вакцины, вошедшее в анналы истории вакцинирования против Hib. Было выявлено, что вакцина крайне эффективна (55-85 % при уровне достоверности в 95 %) в возрасте 18-71 месяцев и обеспечивает 4-летнюю защиту в 90 % случаев. Однако, более скромные результаты были получены у детей в возрасте до 18 месяцев.
Позже проводились многочисленные испытания полисахаридных вакцин в Европе и Северной Америке. В частности, клиническое испытание в Великобритании (1991—1993) показало снижение на 87 % заболеваемости менингитом гемофильной этиологии. В Голландии, при проведении аналогичного исследования, было зафиксировано полное отсутствие случаев менингита гемофильной этиологии в течение 2-х лет после начала иммунизации.
В настоящее время обязательная иммунизация против гемофильной инфекции введена в США (1990), Канаде (1990) и ряде других стран. С 2011 года прививка против Hib включена в российский национальный календарь прививок и предоставляется детям из групп риска[1][2]. Вакцинация проводится детям в 3 этапа: в 3, 4,5 и 6 месяцев. В возрасте 18 месяцев — однократная ревакцинация.
Некоторые факты, подтверждающие эффективность вакцинации[править | править код]
По данным, опубликованным рядом авторов (Adams WG et al) в JAMA, результаты таковы:
- 1989 — 37/100000
- 1991 — 11/100000
Снижение числа случаев заболеваний менингитом гемофильной этиологии у детей на 82 % с 1985 по 1991, предотвращение около 10000-16000 заболеваний гемофильной инфекцией в 1991 году.
В настоящее время наиболее эффективным считается введение трех доз конъюгированных вакцин — в 2, 4 и 6 месяцев. Вакцины взаимозаменяемы.
Примечания[править | править код]
Литература[править | править код]
- Королева И. С. и соавт. Эпидемиологические особенности носительства Haemophilus influenzae типа b. Эпидемиология и инфекционные болезни, № 3, 2000, С.15-19
- Демина А. А. Эпидемиология инвазивных форм заболеваний, обусловленных H.influenzae типа b, Сборник трудов Научно-практической конференции «Актуальные вопросы эпидемиологии, клиники, диагностики и профилактики инфекции, вызываемой H.Influenzae тип b», 1998
- H.A. Bijlmer. Worldwide epidemiology of Haemophilus influenzae meningitis industrialized versus non-industrialized countries. Vaccine, Vol. 9 ; Supplement June 1991, S5-S9. (англ.)
- D.A Clements. Cost of treatment and prevention of Haemophilus influenzae type b disease. Pharmacoeconomics, 1994 ; 6 (5) : 442—452. (англ.)
- R. Booy, et al. Antibody persistence after accelerated immunization against Haemophilus influenzae type b. BMJ, 1993 ; 306 : 971. (англ.)
- R. Gold, et al. Haemophilus influenzae type b disease in Canada: Abstract. Effect of infant vaccination. ISID Congress, 1996. (англ.)
Источник
Гемофильная инфекция — острая антропонозная инфекционная болезнь с аэрозольным механизмом передачи возбудителя, которая характеризуется преимущественным поражением респираторного тракта и оболочек мозга.
Коды по МКБ -10
А41.3. Септицемия, вызванная Haemophilus influenzae (палочка Афанасьева–Пфейффера).
А49.3. Инфекция, вызванная Haemophilus influenzae, неуточнённая.
В96.3. Haemophilus influenzae как причина болезни, классифицируемая в других рубриках.
J14. Пневмония, вызванная Haemophilus influenzae.
Этиология (причины) гемофильной инфекции
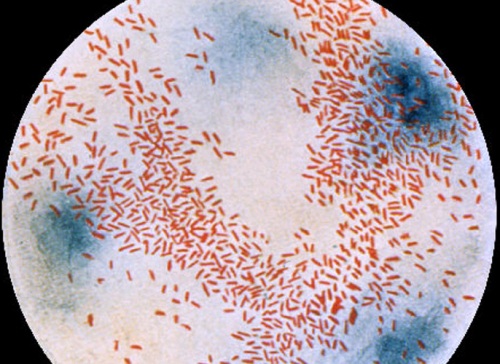
Возбудитель — бактерия Haemophilus influenzae (H. influenzae, син. — палочка Пфейффера). Гемофильная палочка рода Haemophilus (семейства Pasteurellaceae) — мелкая коккобацилла, может иметь полисахаридную капсулу. В окружающей среде неустойчива. Имеет К- и О-антигены. По капсульному антигену выделяют шесть сероваров (а, b, c, d, e, f). Из представителей Hemophilus для человека патогенен только H. influenzae типа b (Hib). Основные факторы патогенности — капсула и пили. Капсула подавляет фагоцитарную активность лейкоцитов, пили обеспечивают адгезию возбудителя к клеткам эпителия. Дополнительные факторы патогенности — IgA-протеазы, расщепляющие секреторные иммуноглобулины.

Фото гемофильной палочки в электронный микроскоп после окраски по Грамму
Возбудитель также содержит липополисахаридный и гликопротеиновый комплекс. Имеются данные о существенной роли ЛПС в патогенезе ИТШ у больных Hib-инфекцией. H. influenzae малоустойчива в окружающей среде. Гибнет в течение 30 мин при температуре 55 °С, под воздействием солнечных лучей и при высыхании. Дезинфицирующие растворы в обычно применяемых на практике концентрациях убивают Н. influenzae через несколько минут.
Эпидемиология гемофильной инфекции
Источник инфекции — больные любой клинической формой Hib-инфекции, а также здоровые носители. Частота носоглоточного носительства гемофилов может достигать 90%, но капсульные штаммы Hib, с которыми связаны почти все случаи болезни, обнаруживают только у 3–5% обследованных.
Основной путь передачи возбудителя — воздушно-капельный; возможен также контактный путь. Восприимчивость человека изучена плохо. Известно, что вероятность заражения у детей от 3 мес до 5 лет в 6000 раз выше, чем в других возрастных группах. По-видимому, высокая восприимчивость детей в возрасте до 5 лет (более 90% больных) обусловлена не только отсутствием иммунитета, но и анатомо-физиологическими особенностями.
Патогенез гемофильной инфекции
Входные ворота инфекции — слизистая оболочка верхних дыхательных путей, где возбудитель может длительно бессимптомно персистировать. С этой локализацией возбудителя связаны ОРЗ, вызванное Hib, эпиглоттит, отит, синусит. Механизм развития гемофильной пневмонии неизвестен. При нарушении или неполноценности механизмов защиты возбудитель преодолевает барьер слизистой оболочки и попадает в кровь. Бактериемия приводит к развитию септицемии (может осложняться ИТШ), артрита, остеомиелита и менингита в результате проникновения возбудителя через ГЭБ. При этом защитные ресурсы организма ограничиваются фагоцитозом, что и объясняет высокую летальность (свыше 50%) в отсутствие адекватной терапии. Гемофильный менингит (Hib-менингит) — наиболее типичная и частая форма Hib-инфекции. В развитии болезни выявляют три фазы:
· фазу респираторной инфекции;
· бактериемию (частота выделения гемокультуры свыше 60%);
· фазу менингита.
Клиническая картина (симптомы) гемофильной инфекции
Инкубационный период Hib-инфекции составляет, по-видимому, от двух до четырёх дней. Единой классификации Hib-инфекции нет. Целесообразно выделять бессимптомное носительство, локализованные [ОРЗ (ринофарингит), ОРЗ, осложнённое синуситом, отитом; флегмона, целлюлит] и генерализованные (инвазивные) формы болезни (эпиглоттит, пнвмония, септицемия, менингит, остеомиелит, артрит).
ОРЗ, выхванные Haemophilus influenzae, существенно не отличаются от ОРЗ другой этиологии, но часто осложняются отитом и синуситом.
Эпиглоттит — воспаление надгортанника, тяжёлая форма Hib-инфекции. Чаще наблюдают у детей 2–7 лет. Начало острое: озноб, высокая лихорадка, слюнотечение. В течение нескольких часов нарастают симптомы ДН (инспираторная одышка, тахикардия, стридор, цианоз, втяжение податливых участков грудной клетки). Больные занимают вынужденное положение. Возможно развитие септицемии, менингита.
Флегмона. Наблюдают у детей до 1 года, наиболее частая локализация — голова и шея. Клинической картиной может напоминать рожу. Возможны бактериемия и менингит.
Целлюлит также наблюдают у детей до 1 года; чаще локализуется на лице и шее. Часто развивается на фоне ринофарингита. В области щеки или вокруг глазницы, на шее появляются гиперемия с синюшным оттенком и отёчность кожи. Общая интоксикация не выражена, но могут присоединиться отит, менингит и пневмония.
Пневмония. Клиническая картина не отличается от таковой при пневмококковой пневмонии. Может осложняться менингитом, плевритом, септицемией.
Септицемия. Чаще наблюдают у детей до 1 года. Характеризуется гипертермией, часто геморрагической сыпью, развитием ИТШ.
Остеомиелит, артрит обычно развиваются на фоне септицемии.
Менингит, вызванный гемофильной палочкой типа b (Hib-менингит), занимает 3-е место по частоте встречаемости в этиологической структуре бактериальных менингитов, составляя от 5 до 25%, а у детей в возрасте до 5 лет — 2-е место (10–50%).
Имея много общих черт с другими видами бактериального менингита, Hib-менингит отличается рядом существенных клинико-патогенетических особенностей, которые необходимо учитывать при ранней диагностике и выборе оптимальной тактики этиотропной и патогенетической терапии. Hib-менингит поражает преимущественно детей в возрасте до 5 лет (85–90%). Часто (10–30%) болеют и дети до 1 года, включая первый месяц жизни. На долю детей старше 5 лет и взрослых приходится 5–10% заболевших. У большинства больных Hib-менингитом развивается на отягощённом преморбидном фоне (органические поражения ЦНС, отягощённое течение второй половины беременности и родов, частые респираторные инфекции в анамнезе, нарушения в иммунной системе). У детей старше 5 лет и взрослых существенное значение имеют анатомические дефекты (spina bifida). Эти больные, как правило, неоднократно болеют бактериальным менингитом различной этиологии.
Болезнь чаще начинается подостро: с кашля, насморка, повышения температуры тела до 38–39 °С. У некоторых больных в начальном периоде могут доминировать диспепсические расстройства. Этот период длится от нескольких часов до 2–4 сут, затем состояние ребёнка ухудшается: усиливаются симптомы интоксикации, температура достигает 39–41 °С, усиливается головная боль, присоединяются рвота, менингеальные симптомы, расстройства сознания, судороги, а через 1–2 дня — очаговые симптомы. При остром начале болезни катаральные явления могут отсутствовать. Болезнь в этих случаях начинается с быстрого повышения температуры тела до 39–40 °С, головной боли, рвоты. Отчётливые менингеальные синдромы появляются на 1–2-й день болезни. В среднем отчётливые признаки поражения ЦНС при Hib-менингите отмечают на 2 дня позже, чем при менингококковом менингите, и на сутки позже, чем при пневмококковом менингите. Это часто приводит к поздней диагностике и позднему началу этиотропной терапии.
Лихорадка при Hib-менингите чаще ремиттирующая или неправильная, регистрируется даже на фоне антибактериальной терапии, длительностью от 3–5 до 20 (в среднем 10–14) сут и более. Уровень лихорадки выше, чем при бактериальных менингитах другой этиологии. Сыпь возможна в отдельных случаях. Катаральные явления в форме фарингита обнаруживают более чем у 80% больных, ринита — более чем у 50% больных. Реже отмечают явления бронхита, у отдельных больных — пневмонию. Часто увеличены селезёнка и печень; аппетит отсутствует, возникают рвота, срыгивание пищи, задержка стула (но возможна диарея). Заторможенность сознания, адинамия, быстрая истощаемость характерны для большинства больных. Реже развивается сопор, в отдельных случаях — кома.
На фоне дегидратационной и адекватной антибактериальной терапии сознание полностью восстанавливается в сроки от 4–6 ч до 2–3 сут. Выраженную картину отёка мозга наблюдают примерно у 25% больных, но признаки дислокации мозга (кома, генерализованные судороги, расстройства дыхания) обнаруживают значительно реже.
В то же время очаговую неврологическую симптоматику обнаруживают не менее чем у 50% больных. Чаще отмечают парезы черепных нервов, ухудшение слуха, фокальные судороги, атаксию, нарушения мышечного тонуса по экстрапирамидному типу, реже парезы конечностей.
Менингеальный синдром (в частности, выбухание родничка), симптом подвешивания выражены умеренно. Ригидность мышц затылка, как правило, характерна для детей старше 1 года, а симптомы Брудзинского и Кернига у части больных слабо выражены или отсутствуют. Картина ликвора характеризуется умеренным нейтрофильным или смешанным плеоцитозом, небольшим повышением уровня белка. Мутность ликвора может быть обусловлена огромным количеством гемофильной палочки, которая при микроскопии занимает всё поле зрения. Содержание глюкозы в первые 1–2 дня варьирует от резкого снижения до повышения уровня, после 3-го дня — менее 1 ммоль/л или глюкоза не определяется.
Картина крови отличается слабо или умеренно выраженным лейкоцитозом: почти у половины больных лейкоцитоз, у остальных — нормоцитоз или лейкопения. У большинства больных — абсолютная лимфопения (до 300–500 клеток в 1 мкл), а также тенденция к уменьшению количества эритроцитов и гемоглобина.
Диагностика гемофильной инфекции
Клиническая диагностика любых форм Hib-инфекции, кроме эпиглоттита, ориентировочная, так как Hib — наиболее частый его возбудитель. Диагноз Hib-инфекции устанавливают на основании выделения гемокультуры возбудителя и культуры из патологических секретов (СМЖ, гной, плевральный выпот, мокрота, мазки из носоглотки). В последнем случае диагностическое значение имеет только выделение капсульных штаммов. Для посева используют шоколадный агар с факторами роста. Для диагностики менингита применяют также бактериоскопию, ПЦР и реакцию РЛА СМЖ.
Дифференциальная диагностика гемофильной инфекции
Эпиглоттит дифференцируют от дифтерии верхних дыхательных путей, крупа при ОРВИ и инородного тела в гортани (табл. 17-38). Другие формы Hib-инфекции отличают на основании результатов лабораторных исследований. Hib-менингит дифференцируют от других видов бактериального, вирусного менингита, менингизма при острых лихорадочных заболеваниях.
Таблица 17-38. Дифференциальная диагностика острого эпиглоттита
| Симптомы | Нозологическая форма | Инородное тело в гортани | ||
| острый эпиглоттит | дифтерийный круп | круп при ОРВИ | ||
| Начало | Бурное | Постепенное | Острое | Внезапное |
| Лихорадка | Высокая | Субфебрильная | Субфебрильная, до 38–39 °С | Отсутствует |
| Интоксикация | Резко выражена | Не характерна | Не выражена | Отсутствует |
| Афония | Охриплость голоса | Афония | Охриплость голоса | Охриплость голоса |
| Стридор | Наблюдается | Не наблюдается | Наблюдается | Наблюдается |
| Катаральные явления | Слабо выражены | Отсутствуют | Характерны | Отсутствуют |
| Саливация | Характерна | Отсутствует | Отсутствует | Не характерна |
| Затруднение при глотании | Характерно | Отсутствует | Отсутствует | Отсутствует |
| Кашель | Возможен | Сухой | Приступо-образный лающий | Приступо-образный |
| Боли при глотании | Характерны | Отсутствуют | Возможны | Возможны |
| Степень стеноза гортани | III–IV | III–IV | I–II | I–II |
| Ларингоскопия | Резкий отёк и гиперемия надгортанника, отёк мягких тканей | Налёты на голосовых связках | Гиперемия, отёк подсвязочного пространства | Инородное тело в просвете или стенке гортани |
Показания к консультации других специалистов
При признаках поражения ЦНС показана консультация невролога, при местных гнойно-воспалительных очагах — хирурга; при признаках стеноза гортани — отоларинголога.
Показания к госпитализации
Клинические: наличие менингеального синдрома, ДН, стеноза гортани, местных гнойно-воспалительных процессов (флегмона, целлюлит, артрит, остеомиелит). Режим в стационаре — постельный.
Пример формулировки диагноза
А41.3. Септицемия, вызванная Hib, гнойный менингит, ОНГМ.
Лечение гемофильной инфекции
Длительность лечения не менее 7–10 сут.
Диета
Стол № 13. При эпиглотитте — стол № 1А, парентеральное или зондовое питание.
Медикаментозная терапия
Этиотропная терапия генерализованных форм болези представлена в табл. 17-39.
Таблица 17-39. Этиотропная терапия генерализованных форм Hib-инфекции
| Препарат | Суточная доза, мг/кг | Кратность введения, раз | Путь введения |
| Препараты первого ряда | |||
| Хлорамфеникол | 25–50, при менингите — 80–100 | 3–4 | Внутривенно, внутримышечно |
| Амоксициллин-клавулановая кислота | 30 | 3–4 | Перорально, внутривенно |
| Цефотаксим | 50–100, при менингите — 200 | 4 | Внутривенно, внутримышечно |
| Цефтриаксон | 20–80, при менингите – 100 | 1–2 | Внутривенно, внутримышечно |
| Препараты второго ряда | |||
| Меропенем | 30, при менингите — 120 | 3 | Внутривенно |
| Ципрофлоксацин | 20, при менингите — 30 | 2 | Перорально, внутривенно |
Для лечения локализованных форм также применяют:
· азитромицин в дозе 10 мг/кг перорально однократно;
· рокситромицин — по 5–8 мг/кг два раза в сутки перорально;
· ко-тримоксазол — по 120 мг два раза в сутки перорально в течение 3 сут.
Патогенетическую терапию назначают, основываясь на клинических показаниях, и проводят по общим правилам. При менингите показана дегидратационная терапия (фуросемид, ацетазоламид в средних терапевтических дозах; дексаметазон в дозе 0,5 г/кг в сутки внутривенно или внутримышечно).
При ОНГМ применяют ИВЛ, оксигенотерапию, противосудорожные средства.
При остром эпиглоттите показаны интубация трахеи, петлевые диуретики, глюкокортикоиды, антигистаминные препараты.
При местных нагноительных процессах (флегмона, остеомиелит) используют хирургические методы лечения.
Прогноз гемофильной инфекции
При менингите, септицемии, эпиглоттите — серьёзный, при остальных формах Hib-инфекции — благоприятный. После менингита возможны стойкая тугоухость, гидроцефально-гипертензивный синдром.
Сроки нетрудоспособности при менингите составляют 1–2 мес после выписки из стационара.
Диспансерное наблюдение
При Hib-менингите показано. Осуществляет невролог, продолжительность не менее 1 года.
Профилактика гемофильной инфекции
Специфическую профилактику проводят по индивидуальным показаниям (частые ОРВИ, патология беременности и родов у матери, поражения ЦНС у ребёнка). Применяют вакцины:
· Акт-ХИБ (Франция) в дозе 0,5 мл внутримышечно или подкожно (с 2–3 до 6 мес — троекратно с интервалом 1–2 мес с однократной ревакцинацией через 1 год; от 6 до 12 мес — двукратно с интервалом 1 мес и ревакцинацией через 18 мес; от 1 года до 5 лет — однократно);
· Хиберикс (Бельгия) в дозе 0,5 мл подкожно или внутримышечно (от 3 нед до 6 мес — троекратно с интервалом 1–2 мес и ревакцинацией через 1 год; от 6 мес до 1 года — двукратно с интервалом 1 мес и однократной ревакцинацией через 18 мес; от 1 года до 5 лет — однократно).
Источник
